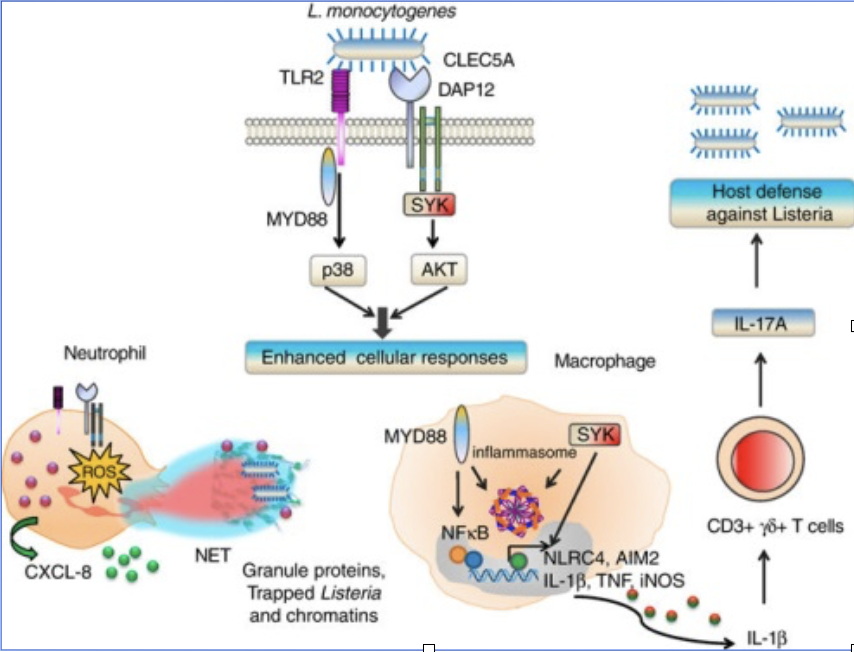
李斯特菌引起之C型凝集素5A與TLR2共同活化,可增強宿主免疫對抗李斯特菌感染。(圖片來源:臺灣聯合新聞網)
中國臺灣網8月24日訊 據臺灣《經濟日報》報道,臺灣“中研院”研究基因體中心特聘研究員謝世良團隊發現,C型凝集素5A(CLEC5A)基因,是細菌侵入體內時,引發嗜中性白血球胞外捕捉(Neutrophil Extracellular Trap,簡稱NET)的關鍵,而過大的NET風暴,則被認為是紅斑性狼瘡等免疫疾病的主因。因此,未來若能近一步阻斷CLEC5A基因的表現,有望治療此類免疫疾病。
“嗜中性白血球(Neutrophil)”在人體免疫係統內,扮演著嫉惡如仇的角色,當侵入人體的細菌數量太多,嗜中性白血球無法藉由吞噬細菌來抑制細菌入侵時,它們會傾全力將自身的細胞核膨脹,釋出脫氧核糖核酸(DNA),然後“壯烈成仁”。DNA是帶負電荷黏性很強的物質,因此這奮力一搏,就如同天羅地網般,可將入侵細菌一網打盡,此過程稱為NET。
謝世良團隊發現,CLEC5A正是細菌引發NET的重要因子,研究團隊用“李斯特菌”、“金黃色葡萄球菌”與各式的“基因剃除鼠”做實驗,發現只有CLEC5A基因剃除鼠在細菌感染後,負責調控NET的PAD4酵素不會有活化現象,也沒有發生NET。
然而過度的NET卻可能帶給患者更大的災難。許多自體免疫病症,都在細菌感染治愈之後出現,這是由于過多NET反而刺激免疫係統產生過量的甲型幹擾素(interferon-alpha),造成自體免疫的病症。例如紅斑性狼瘡(systemic lupus erythematosus,簡稱SLE)的患者,在發病前往往有發炎感染的狀況,當引發自體免疫反應時,中性白血球數量急速下降,體內的幹擾素(interferon)極高,PAD4酵素也被活化,即表示有過多的NET產生。
此外,研究團隊還發現,在腸道免疫病患者發炎時,有一種叫“IL-17 γδ-T cell”細胞,會產生IL-17A細胞激素,但若剔除CLE5A基因,IL-17 γδ-T cell就會消失。由于這群細胞在腸道先天免疫力扮演重要角色,被認為與發炎性腸道疾病(inflammatory bowel disease, IBD)息息相關,因此阻斷CLEC5A或許也有治療此疾病的功效。
原被科學家看好,屬于“類鐸受體”的TLR2,是對抗“格蘭氏陽性菌”的主要受體,但經科學界多年的檢驗,此論點似乎並不盡正確。謝世良表示,基于CLEC5A在NET所扮演的角色,顯示此基因為極具潛力成為治療目標。研究團隊將持續對各種細菌進行詳盡分析,鑒定出所有與CLEC5A有直接關係的細菌及各種微生物,可望帶來治療新希望。
過去,C型凝集素5A(CLEC5A)基因已被證實和登革熱、禽流感患者所產生的細胞風暴現象有直接的關聯,也是登革病毒及禽流感病毒造成人類死亡的重要致死因子。
臺灣“中研院”研究基因體中心特聘研究員謝世良團隊進一步研究CLEC5A在對抗細菌感染時的角色,發現此基因是比“類鐸受體(Toll-like receptor 2- TLR2)”更關鍵的防衛因子,未來可望成為細菌感染療法的新方向。
此重要發現于8月21日發表于《自然通訊》(Nature Communications) 期刊,第一作者為臺灣陽明大學陽明臨床醫學研究所助理教授陳斯婷,謝世良為通訊作者。(中國臺灣網 王怡然)
[責任編輯:王怡然]